新型態藥物發展
新型態藥物發展
再生醫療CDMO大廠樂迦再生科技(5)日宣布,繼竹北「智慧細胞工廠」正式啟用後,公司已成功發展出「一次性病毒感測數位晶片技術」,目前正全面布局美國、歐洲、日本與台灣等地的獨家專利,為全球細胞製程品質樹立全新數位化標準。...
興櫃生技股啟新生技(7837)18日宣布,斥資5億元於新竹生醫園區建置逾650坪的新廠,於18日舉行竹北生醫園區新廠開幕典禮,正式啟用符合國際等級PIC/S GMP規範設計的細胞培養基製造基地,並導入以藥廠專用Isolator隔離系統為核心的製程平台,宣示啟新生技正式強化再生醫療產業供應鏈的布局。...
再生醫療大廠樂迦再生(6891)12日宣布,已於3月10日與美國委託臨床(CRO)大廠Charles River Laboratories簽署合作備忘錄(MOU),雙方未來將在台灣與亞太地區,就細胞製造CMC、分析測試、技術研發以及相關新型療法的研發進行合作。...
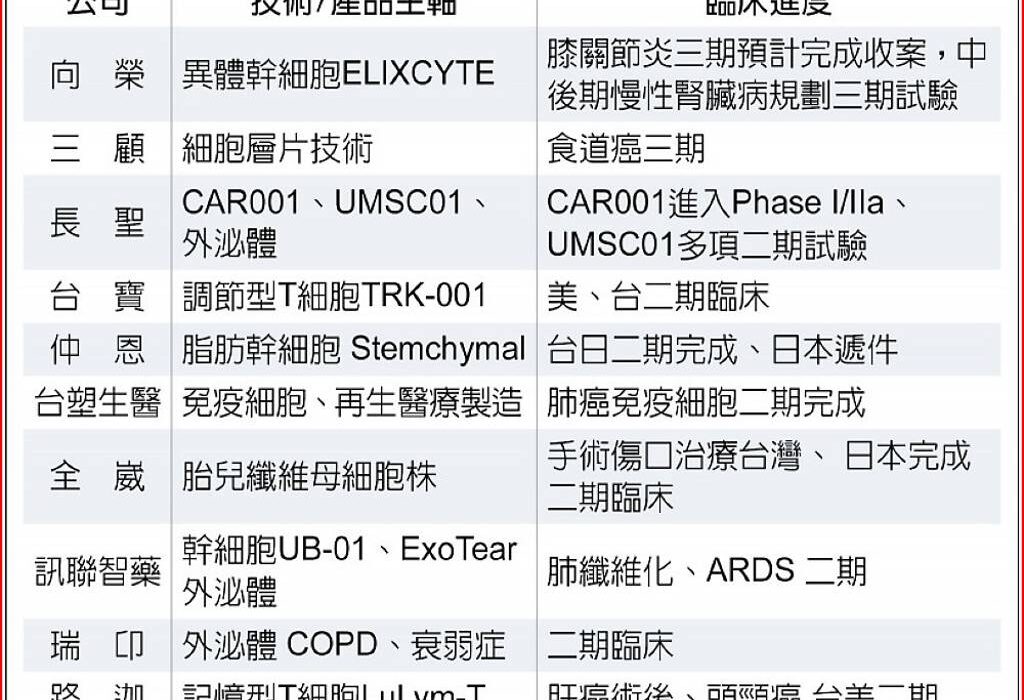
《再生醫療雙法》2026年正式上路,為台灣細胞治療產業打開制度性突破口。新制首度明定,細胞新藥完成第二期臨床試驗後,即可申請為期五年的暫時性藥證,等同大幅縮短上市時程,被法人圈視為再生醫療產業的「關鍵拐點」。在政策紅利加持下,臨床試驗、國際授權與CDMO製造三大動能同步啟動,並進入黃金成長期。...
興櫃生技股仲恩生醫(7729)14日公告,與日本再生醫療產業夥伴Cyto-Facto正式簽署合作意向書(Letter of Intent, LOI),雙方將就仲恩核心幹細胞產品Stemchymal委託製造合作展開密切洽談,為未來日本取證後之市場供給預作準備,並作為仲恩深化台日再生醫療產業鏈合作的重要一步。...
醣聯 (4168)8日宣布,與日本東京科學大學及Change Cure簽署抗體製造委託服務協議,將委託醣聯製造CC001 (Anti-HMGB1單株抗體)之臨床試驗用藥、並協助在日本申請治療大腦退化性疾病─前額葉顳葉變性症(FTLD)的臨床1/2a期試驗。...
讀者專欄
在生技製藥領域內,法規人員(Regulatory Affairs,RA)的職務內容會因應公司產業、產品類別或產品正處於的生命週期而有所差異,但終極目標不會改變:確保醫藥產品合規並達成預期所訂定的目標,如IND、NDA或產品上市等目的。...
藥廠法規人員(Regulatory Affairs,RA)不僅是藥廠與衛生主管機關之間的溝通橋樑,更是推動藥品從研發到上市,乃至後續許可證維護的重要推手。透過對藥品查驗登記等法規制度的深入理解,RA 協助藥廠進行產品的生命週期管理,確保每一步皆符合各國監管機構的法規要求,進而保障民眾的用藥安全與公共健康。...
隨著細胞治療技術的快速發展,許多再生醫療業者面臨如何將此新興生醫技術成功商業化的挑戰。再生醫療業者可採取多元化策略,包括與技術領先者合作進行產品研發與技術轉移,運用現代化的調整性臨床試驗設計加速產品的開發過程,並通過了解與利用細胞療法的加速上市法規政策,達成搶占市場商機目標。...